El cloro, el pH y su relación con el Ácido Isocianúrico

Desde el principio se nos enseñó que el pH determina el porcentaje de ácido hipocloroso siendo el componente desinfectante, o la fuerza del cloro. Y eso es cierto, excepto cuando existe acido isocianurico en el agua. El CYA cambia completamente las reglas del juego. Por cierto, este es un tema que puede causar controversia, pero toda la información está respaldada por investigaciones y sus fuentes respectivas.
El pH realmente controla la fuerza de desinfección del cloro?
Los libros de texto y diversas fuentes de información en la industria nos enseñan que un pH más bajo significa un cloro más fuerte. Eso es únicamente cierto sin la existencia de CYA en el agua. Gracias a algunas investigaciones del Dr. Stanley Pickens y el resto del comité AD-HOC de CMAHC sobre el ácido isocianúrico, ahora sabemos que el CYA rige el control de la fuerza del cloro sin importar tanto el pH. Aunque el pH sigue siendo críticamente importante para el equilibrio del agua en el ISL.
Pero es importante tener en cuenta que esta información ha sido conocida y publicada desde 1974. Simplemente nunca fue ampliamente adoptada en la industria de las piscinas. Esta no debería ser información nueva, pero decidimos desarrollar este artículo porque cuando hablamos al respecto, todos parecen estar sorprendidos.
Fuerza o poder del cloro (% HOCl)
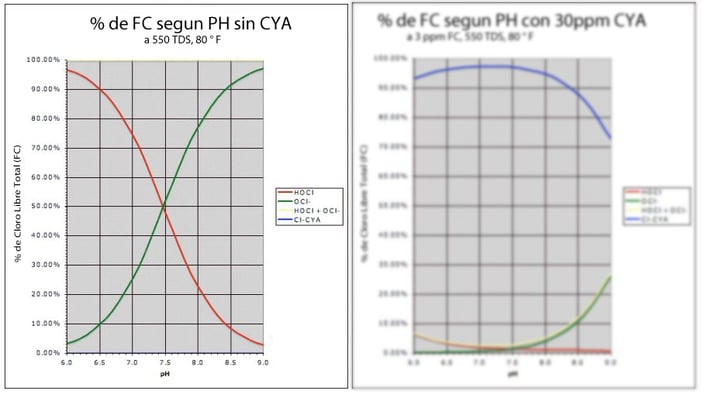
En la siguiente grafica podemos observar el porcentaje de ácido hipocloroso o fuerza del cloro con respecto al nivel del pH. Cuanto más bajo es el pH, mayor es el porcentaje del componente más desinfectante del cloro, el ácido hipocloroso (HOCl). Cuanto mayor sea el pH, menor será ese porcentaje, ya que el HOCl está en equilibrio con la forma mucho más débil de cloro, el ion de hipoclorito (OCl-). Estas gráficas fueron recreados y tomados del libro de Richard Falk sobre el cloro y el CYA. La información proviene originalmente de un estudio realizado en 1974 por J. O'Brien et.al., citado al final de este artículo.1
La línea roja es el cloro fuerte HOCl, y la línea verde es cloro débil OCl-. Con un pH de aproximadamente 7.5, se tienen aproximadamente 50-50. Pero con un pH de aproximadamente 7.2, es un 70% de cloro fuerte. Entonces sí, en este caso, el pH controla la resistencia del cloro (% HOCl). Por lo cual no es raro que los libros de texto de la industria nos digan que el rango de pH deseado para piscinas es de 7.2-7.8. Pero eso es para piscinas sin CYA. Mire el título, donde dice en negrita "... sin CYA". Aquí está el otro lado de la gráfica con solo 30 ppm de CYA en el agua:
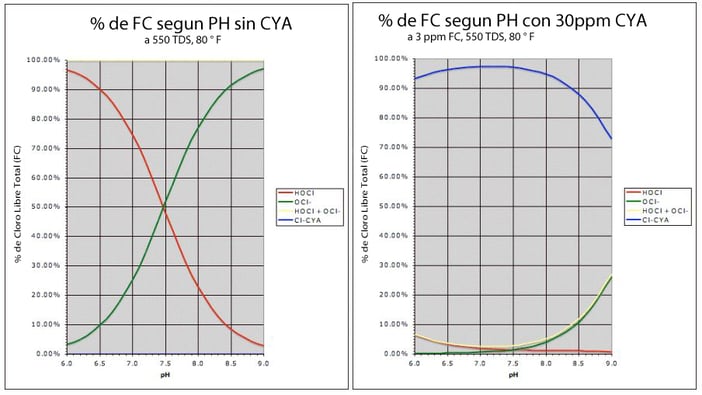
Alguna diferencia?
¿Dónde está la línea roja? Hay mucho que analizar en este gráfico, pero este es el resumen: el CYA ha asumido el papel del pH para controlar la fuerza y la velocidad del cloro. Si la fuerza se determina por el % de HOCl, este cae por debajo del 3% a un pH de 7.5, en comparación con un 50% de fuerza de cloro sin la existencia de CYA al pH de 7.5. Lo que sucedió aquí es simple: el cloro se ha unido al CYA creando isocianuratos (representados por la línea azul, Cl-CYA en el gráfico). La línea amarilla es una combinación de todo el cloro que no está unido al CYA. Como puede ver, la gran mayoría del cloro se une al CYA a 30 ppm. Podemos concluir lo siguiente:
- Primero, solo 30 ppm de CYA se unen a la gran mayoría del cloro, lo que lo protege de la luz solar, por lo que la idea de tener un CYA por mucho más arriba de 30 ppm es un error, a menos que tenga niveles más altos de cloro libre que lo acompañen.
- En segundo lugar, en presencia de CYA, la mayoría del cloro tiene que desprenderse antes de desinfectar u oxidar, lo que aumenta el tiempo de contacto (CT).
Como el pH de la piscina debería [normalmente] oscilar entre 7.2 y 8.2, como puede ver, casi no hay diferencia en el porcentaje de HOCl entre un pH de 7.0 y 9.0 cuando existe CYA en el agua de la piscina.
Para que no se le olvide, prácticamente no hay diferencia en la concentración de cloro (% HOCl) en función del pH cuando CYA está presente en la piscina.
Sabemos que durante años se nos ha dicho lo contrario, intentando mantener un pH entre 7.4 y 7.6, cuando en realidad el agua ni siquiera desea mantenerse allí. Pero la verdad es que el pH no controla la fuerza de cloro cuando existe CYA en la piscina, sino la relación de cloro libre con acido isocianurico (CL:CYA)
Perseguir el pH es un error
Nos hemos dado cuenta que el pH es difícil de mantener en un nivel fijo, gracias a que fluctúa muy fácilmente con casi cualquier cosa. Hay una gran variedad de cosas que causan un alto pH en la piscina, como lo discutimos en este artículo. Es por eso que hemos desarrollado una mejor manera para contener el pH en lugar de controlarlo.
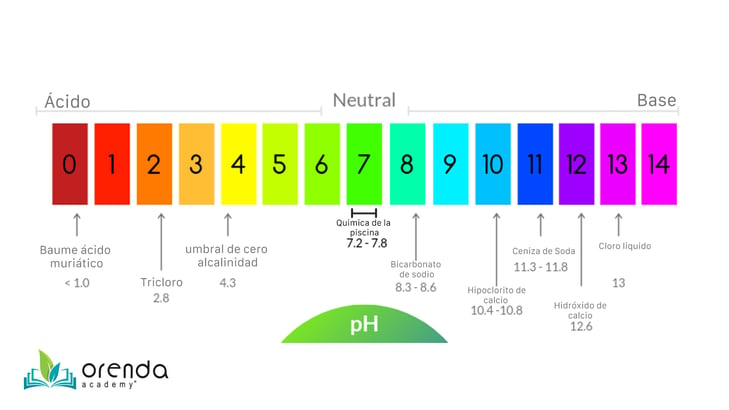
La tabla anterior muestra la escala del pH y los productos químicos comunes utilizados. Cuando considera las diferencias extremas en el pH de estos productos químicos, ¿es de extrañar por qué el pH rebote cuando intenta controlarlo? Tenga en cuenta que la ceniza de soda es aproximadamente 1200 veces más básica que el bicarbonato de sodio. ¿Cuál cree que es la diferencia entre el ácido muriático y el cloro líquido?
Es difícil mantener el pH fijo en un valor porque está en un equilibrio que fluctúa rápidamente cuando se agregan productos químicos de ajuste de pH a la piscina. También sabemos que el pH depende en gran medida de la cantidad de dióxido de carbono (CO2) disuelta en el agua. Así que cuando el CO2 deja el agua, el pH aumenta. Por eso mismo, las piscinas o albercas que cuentan con fuentes o cascadas o bordes infinitos tienen a tener un pH ligeramente mayor que la piscinas sin estas características.
CO2 y la ley de Henry
También sabemos que el pH solo puede elevarse naturalmente hasta cierto punto, gracias a la ley de solubilidad de gases de Henry. Básicamente establece que la concentración de un gas sobre una superficie de un líquido estará en equilibrio con la concentración de ese mismo gas en el líquido de manera soluble. Dado que el pH está determinado por la cantidad de CO2 en el agua, el porcentaje de CO2 en el agua eventualmente se igualará con el porcentaje de CO2 en el aire sobre la piscina. Cuando el dióxido de carbono llega al equilibrio, se dice que ha llegado al techo del pH, el cual también depende naturalmente de la alcalinidad de carbonatos o alcalinidad corregida en el agua, como se muestra en la siguiente tabla:
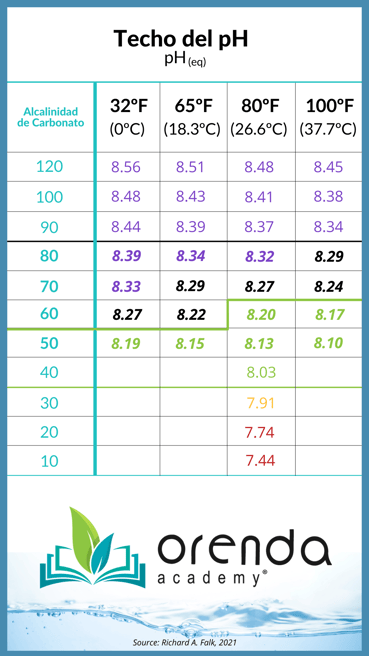
Fuente: Richard A. Falk
Los números en negrita en el centro de la tabla muestran los rangos de alcalinidad de carbonato más comunes en las piscinas. Esto es importante, porque cuando el pH supera los 8.2, se vuelve mucho más difícil que el carbonato de calcio permanezca en solución (el ISL es demasiado alto, por lo general). Esto es parte de por qué en Orenda recomendamos un mayor nivel de dureza de calcio y menor alcalinidad, entre 60-90 ppm, en lugar de hasta 120 ppm2. Nota: no permita que su alcalinidad baje tanto si hace que su ISL se vaya por debajo de -0.30. Esto solo debe hacerse con suficiente dureza de calcio para compensar el nivel de alcalinidad más bajo.
El punto es, el pH de la piscina aumentará naturalmente si no se agregan productos químicos. Es la física, y no va a cambiar. No está haciendo nada malo si su pH sigue subiendo. Es importante saber que si el pH supera su techo natural (~ 8.2), entonces fue forzado de forma antinatural.
Mayor CYA significa menor alcalinidad de carbonatos
Una vez más el pH y el CYA se ven relacionados de alguna forma. Un CYA más alto significa más alcalinidad de isocianurato, la cual debe restarse de su alcalinidad total para encontrar la alcalinidad de carbonatos. Es complicado, lo sabemos, pero no se preocupe. La aplicación Orenda calcula todo esto por usted cuando ingresa sus números de CYA y de alcalinidad total en la calculadora.
Así como para calcular el ISL, se toman en cuenta factores de corrección. Lo mismo ocurre con la alcalinidad de isocianurato:
-1.png?width=2000&name=ISL%20Equivalents%20chart%20(espanol)-1.png)
Dependiendo del pH, el factor de corrección se encuentra entre 0.23 y 0.36. Digamos que con un pH de 7.6 el factor de corrección es 0.33. Entonces, si tenía 60 ppm de CYA, multiplicado por el factor de conversión nos da 20 ppm y le restamos eso a la alcalinidad total. Una piscina con 90 ppm de alcalinidad total y 60 ppm de CYA tendrá 70 ppm de alcalinidad de carbonatos o alcalinidad corregida. De acuerdo con la tabla anterior de Falk, eso significa que el techo del pH será 8.27 a una temperatura de 80 ºF.
Cómo contener el pH
Si en lugar de tratar de controlar el pH en un nivel fijo, podemos contenerlo a un valor límite nuestra vida será mucho más sencilla. Es por eso que desarrollamos este artículo. Básicamente se trata de establecer una estrategia de equilibrio del ISL con un nivel un poco más bajo de alcalinidad para poder predecir el valor que el pH alcanzara sin salirse del equilibrio. Además que como ya se concluyó, no será forzosamente necesario mantener un pH de 7.4 y 7.6 si existe CYA en el agua.
Y si está pensando que el pH de la piscina tiene que estar en ese nivel para la comodidad del usuario o algo por el estilo, tiene que saber que ese es solo un mito pero, entonces cuál es el pH ideal? El pH ideal es aquel que se ajuste a sus necesidades, su tipo de cloro, de piscina y la temperatura de la zona donde vive. La irritación de los ojos y la piel no es causada por los cambios en el pH, es causada por subproductos de desinfección como las cloraminas y trihalometanos (THM) como el cloroformo.
Como el ácido isocianúrico controla la fuerza del cloro
Se han publicado numerosos estudios en línea que muestran el impacto que el CYA tiene sobre el cloro. Específicamente acerca de cómo el CYA reduce drásticamente la velocidad de acción del cloro (lo que aumenta el tiempo de contacto para la desinfección). Mostramos en las gráficas al comienzo de este artículo cómo las concentraciones de HOCl caen por debajo del 3% con solo 30 ppm de CYA. Eso es increible! Y cualquier propietario y operador de piscinas que use CYA debe ser consciente de ello. Es por eso que el centro de control de enfermedades de los Estados Unidos ha establecido un límite CYA para las piscinas recreativas.
La buena noticia es que el cloro estabilizado (cloro unido al CYA) todavía puede desinfectar. Solo que toma un poco más de tiempo porque el cloro tiene que separarse del CYA antes de que pueda hacer su trabajo. Entonces la estabilización no es el problema aquí; La sobre estabilización es el problema que debe evitarse. La sobre estabilización ocurre cuando se tiene más CYA del que se necesita, y el cloro comienza a hacerse demasiado lento. No necesariamente lo hace más débil (las concentraciones de HOCl ya estaban por debajo del 3% con solo 30 ppm de CYA), pero un cloro más lento significa que la desinfección lleva más tiempo.
El centro de control de enfermedades (CDC) siguiendo el Código Modelo de Salud Acuática (CMAHC) creó un comité AD-HOC para estudiar los efectos del ácido isocianúrico, específicamente para aprender más sobre su impacto. En 2017 publicaron este informe en la Conferencia Mundial de Salud Acuática. Aquí hay una captura de pantalla que consideramos importante de su presentación:
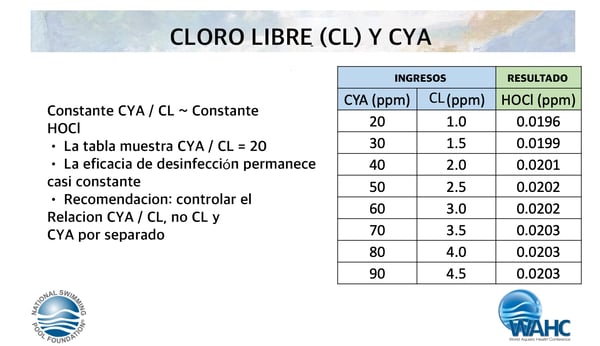
Observe que la concentración efectiva de HOCl es prácticamente la misma, siempre que mantenga la relación de los niveles de cloro libre y CYA.
Gracias a este codigo, la relación de cloro libre y acido isocianurico presentes en el agua está en camino de ser adoptada como el nuevo estándar en lugar de los límites generales de ppm de CYA,o de cloro libre. La desinfección efectiva es el nombre del juego, después de todo. Y si la relación CL y CYA dicta la eficacia del cloro, entonces debe tener eso bien presente. Es por eso que el Modelo de Código de Salud Acuática recomienda un máximo de solo 15 ppm de CYA en una piscina comercial en caso de que exista un incidente fecal. De esta manera el cloro no será tan lento y podrá atacar las bacterias de manera adecuada para prevenir enfermedades. Según este informe de la CDC, este es el tiempo que le toma al cloro eliminar estos patógenos del agua.

Y una vez que se agrega CYA, esto tarda incluso más tiempo. Aquí está el PDF de la respuesta oficial a incidentes Crypto del CDC cuando CYA está presente en la piscina.
Conclusión
El objetivo de este artículo era establecer la relación entre el cloro y el pH, cuando no hay CYA y cuando si hay acido isocianurico en el agua. Claramente, cuando el ácido isocianúrico está en el agua, este manipula la fuerza y velocidad de desinfección del cloro. Las gráficas al comienzo de este artículo muestran que el componente de desinfección del cloro (% de HOCl) es prácticamente el misma de 7.0 a 8.5 cuando existe CYA. Eso significa que el pH ya no es un factor relevante en cuanto al poder de desinfección del cloro; CYA lo controla una vez que está en el agua. Y esa es parte de la razón por la cual tener un CYA mínimo es nuestro cuarto pilar o base del cuidado proactivo de la piscina.
La relación de cloro libre a ácido isocianúrico (CL: CYA) es primordial para una desinfección efectiva en piscinas o albercas. Es más importante que la concentración de cloro libre en ppm. En resumen, el ácido isocianúrico cambia fundamentalmente las reglas para la desinfección.
Sin embargo es importante remarcar que el pH sigue siendo el más dominante de los seis factores del ISL, por lo que es muy importante para el equilibrio del agua en su alberca o piscina. Pero también sabemos que el pH fluctúa muy fácilmente y por eso es relativamente imposible mantenerlo en un valor fijo. En cambio, recomendamos contener el pH utilizando su valor de techo natural (basado en la física y la alcalinidad de carbonatos o alcalinidad corregida) y una base de equilibrio del ISL.
Una ultima cosa, este artículo se trata acerca de piscinas que usan cloro al aire libre o descubiertas. Las piscinas cubiertas no necesitan CYA ya que se usa para proteger el cloro del sol.
1 J. O'Brien, J. Morris y J. Butler, "Equilibrios en soluciones acuosas de isocianurato clorado", Capítulo 14 en A. Rubin, ed., Química del suministro, tratamiento y distribución de agua, Simposio de 1973, (publicado en 1974 ), Ann Arbor Science, Ann Arbor, MI, págs. 333-358.
2 La excepción aquí es durante el Arranque Orenda™, dónde queremos un ISL positivo de +0.20 a +0.30 durante los primeros tres días. Esto generalmente requiere un mínimo de 100 ppm de alcalinidad. Una vez que el cloro y otros productos químicos se introducen en la piscina, la estrategia química debe cambiar hacia un equilibrio ISL más cercano a 0.00.