CO2 y el pH: La ley Henry

Este tema es muy interesante y es justo que le demos la atención adecuada y hablemos de manera extensa además de solo mencionarlo brevemente en nuestros otros artículos pasados acerca del pH. Aunque se escucha complejo, es en realidad uno de los conceptos más fáciles de entender en la química de una piscina.
En este articulo:
- El dióxido de carbono determina el pH del agua.
- Reducir el ph, aumenta el CO2
- Aumentar el pH, significa reducir el CO2
- Ley de Henry de la solubilidad de los gases
- Cómo contener el pH (sin pelear)
- Enfoque principal en el pH
- Mida y dosifique el ácido de manera precisa.
- Conclusión
El dióxido de carbono determina el pH del agua
Lo primero es lo primero: se ha establecido que la cantidad de dióxido de carbono (CO2) en la solución determina el pH del agua. Dicho esto, la razón más común de acidez en el agua es el CO2 disuelto , por lo que cuanto más CO2 existe en el agua, menor será el pH. Esto se debe a que cuando el CO2 se vuelve acuoso en el agua, una pequeña cantidad se convierte en ácido carbónico (H2CO3). La reacción química es desarrollada de la siguiente manera:
CO2 (aq) + H2O → H2CO3 (aq)
Dióxido de carbono + Agua produce ácido carbónico
El ácido carbónico reduce el pH del agua. Y el ácido carbónico se forma cuando el CO2 se introduce en el agua... así que la pregunta es ¿cómo obtenemos más CO2 en el agua para reducir el pH? Bueno, hay que analizar primero cómo se reduce el pH en una piscina.
Reduciendo el pH
Químicamente hablando, podemos reducir el pH de varias maneras, por ejemplo aumentando la cantidad de ácido carbónico en el agua. Primero, se puede inyectar el CO2 directamente en el agua, lo que reduce el pH pero no reduce la alcalinidad. La adición de ácido, por otro lado, reduce el pH y la alcalinidad, porque para que se pueda crear ácido carbónico, el ácido tiene que convertir la alcalinidad del bicarbonato en ácido carbónico con la simple adición de hidrógeno.1 En la siguiente tabla, se muestra como el ácido convierte el bicarbonato (HCO3) en ácido carbónico (H2CO3) en función del pH. Cuando se convierte el bicarbonato, se reduce la alcalinidad total y de carbonato. La inyección del CO2, sin embargo, evita el incremento de alcalinidad y agrega directamente el ácido carbónico a la piscina.
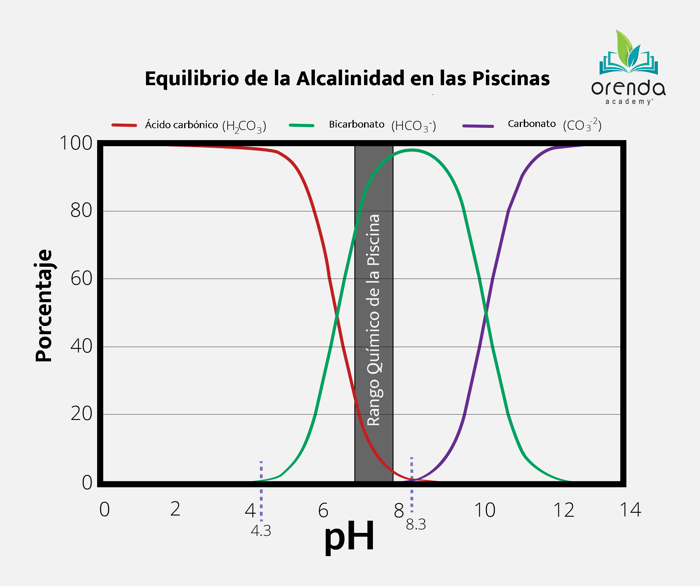
Elevando el pH
Lo opuesto también aplica. El pH aumentará a medida que se reduzca el CO2 en el agua. Se puede realizar esto agregando sustancias de pH alto como cloro no estabilizado, usando un generador de cloro salino o un ajustador de pH como la ceniza de soda (carbonato de sodio) o bicarbonato de sodio2 . También se puede elevar el pH de manera natural a través de la liberación de gases. Hay aireación natural y hay aireación acelerada, como los jets de los spa, aliviaderos, bordes de cascada (piscinas infinitas) y otras características cosméticas en los múltiples diseños. A medida que el CO2 se libera del agua, a través de la aireación o el consumo de algas, el pH aumentará naturalmente. En realidad, es en la pérdida del CO2 en donde entra en juego la Ley de física de Henry.
Si tiene dudas acerca de la alcalinidad o el pH y cómo se relacionan en la química de su piscina, puede leer este artículo.
Ley de Henry de la solubilidad de los gases
La Ley de física de Henry, formulada por William Henry en 1803 establece:
"En temperatura constante, la cantidad de gas que se disuelve de un tipo y volumen específico de un líquido es directamente proporcional a la presión parcial de ese gas en equilibrio con ese líquido". Otra forma de interpretar la ley es que la solubilidad de un gas en un líquido es directamente proporcional a la presión parcial del gas sobre el líquido . (Énfasis agregado) 3
En cuanto a las piscinas, lo que estamos analizando es el CO2. La ley de Henry básicamente nos dice que la cantidad de gas disuelto en el agua se esforzará por ser directamente proporcional a la cantidad de ese mismo gas en el aire sobre el agua. En el caso del CO2, la atmósfera sobre una piscina tiene un pequeño porcentaje de CO2, por lo que el CO2 se libera del agua de la piscina hasta que encuentre equilibrio con el aire. Este video (en ingles) lo explica muy bien. Puede ver el video completo, pero en lo que respecta a este artículo, realmente solo nos importan los primeros dos minutos.
Una vez que se alcanza el equilibrio, la liberación de gases se detiene
La ecuación de la ley de Henry también funciona en el sentido opuesto. Una vez que se alcance el equilibrio, los gases que salen del agua dejarán de emitirse. Explicaremos por qué esto es importante en la siguiente sección (o simplemente puede ir directamente ahí). Claro, la aireación puede forzar temporalmente al CO2 a salir del agua, pero según a la ley de Henry, este será atraído nuevamente al agua y se disolverá. Citando una de nuestras fuentes:
"El dióxido de carbono ingresa al agua a través del equilibrio con la atmósfera. CO2 (aq) << CO 2 (g)" 1
Debido a la Ley de Henry, sabemos que el pH solo puede subir hasta un cierto punto de forma natural, porque la presión atmosférica empujará el CO2 de regreso a la piscina en cierto punto. Si el pH se está elevando por encima de ese punto, ya no es acción natural.
El techo de pH
Con la ley de Henry, sabemos que el CO2 se liberará hasta que alcance el equilibrio con el aire sobre la piscina. Ese punto de equilibrio es básicamente un límite superior o un "techo". Dado que el pH aumenta cuando el CO2 se libera del agua, lo llamamos el techo de pH de la piscina. Sin embargo es posible que el pH pueda elevarse absolutamente por encima de este límite, pero no de forma natural. Algo debe forzar el pH por encima del nivel superior, cómo que se empiece a descomponer una superficie de yeso rica en calcio, aumentando incluso más el pH, o alguien agregando ceniza de sosa a la piscina de manera incorrecta.
El techo o el nivel superior del pH en las piscinas suele ser de alrededor de 8,2, lo que explica por qué casi todas las piscinas se enfrentan de forma natural a un aumento de pH casi de manera semanal. El dióxido de carbono se libera naturalmente gracias a la física, así que no es su culpa como operador! El techo del pH exacto depende de su nivel de alcalinidad de carbonato (o alcalinidad corregida) 4, si quiere saber más acerca de la alcalinidad corregida o porque le decimos asi, puede aprenderlo en este artículo.
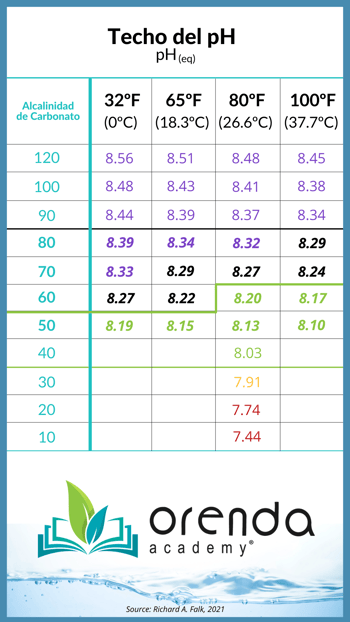
Fuente: Richard A. Falk
Tomando en cuenta que la mayoría de los niveles de alcalinidad de carbonato en piscinas bien mantenidas están entre 50 y 80, puede comparar estos valores en la tabla en negrita. Cuanto más se acerque el pH al valor del techo, más lentamente aumentará el pH. De manera contraria, cuanto más baje el pH por debajo de este valor, más rápido comenzará a subir. Por lo tanto, corregir a 7.2 en lugar de a 7.5 generalmente conduce a un rebote más rápido del pH.
Cómo lidiar con el pH (sin pelearse)
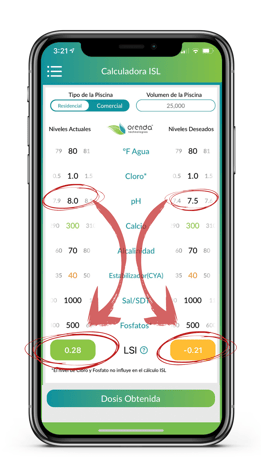
Puede preguntarle a cualquier profesional del negocio qué tan fácil es mantener un pH de 7,4 a 7,6 por una semana. Probablemente se van a reír. Cualquier persona con experiencia sabe que sin la automatización química, es prácticamente imposible mantener ese rango de pH durante una semana completa, excepto en algunas circunstancias raras, como las piscinas de revestimiento de vinilo o fibra de vidrio que usan tricloro. Pero esa es otra historia completamente diferente.
Intentar controlar el pH es inútil. En cambio, ajuste los cambios. Con la Ley de Henry de nuestro lado sabemos que hay un techo de pH y también sabemos que el aumento del pH se ralentiza a medida que se acerca a su techo natural. En el transcurso de una semana, la mayoría de las piscinas no alcanzarán su techo, pero tendrán un pH de aproximadamente 8.0 u 8.1. En este artículo hablamos detalladamente cómo lidiar y contener el pH en un rango en lugar de intentar forzarlo a estar en un punto fijo.
Piense en el ISL
Configure sus parámetros del ISL como el calcio y alcalinidad para permitirle bajar el pH a 7.5 o 7.6 y tener el valor del ISL en amarillo . En temperaturas de agua cálidas, encontrará que esto es más fácil con una cantidad decente de dureza de calcio y una alcalinidad ligeramente inferior, de 60 o 70 ppm. Recuerde en la tabla anterior, la alcalinidad de carbonato determina el techo de pH. Puede observar los valores ejemplares a la captura de pantalla que se muestra en la parte superior.
Hay que asegurarse de que el pH alto o de techo permanezca en verde en la calculadora del ISL de Orenda. En la captura de pantalla, usamos 8.0, basado en el hecho de que la alcalinidad de carbonato del ejemplo tiene un techo de pH de aproximadamente 8.2. Si se hace bien, el pH aumentará muy lento para el final de la semana y esto no lo dejará alcanzar el techo en siete días.
En resumen, use la aplicación Orenda y baje el pH hasta un valor del ISL amarillo (no rojo), y déjelo subir hasta 8.0 u 8.1 mientras permanece en verde (no púrpura).
Mida y dosifique el ácido correctamente
 Para que esta estrategia funcione correctamente, no se puede dar la libertad de exagerar la medición y la dosificación correcta del ácido. Es sumamente crítico. Una alcalinidad más baja reduce la capacidad amortiguadora del agua, por lo que medir el ácido es indispensable para evitar problemas y también es importante que vierta el ácido correctamente con dilución previa. Es sorprendente que tan seguido se usa el ácido en exceso o de manera incorrecta, así como entre otros terribles hábitos comunes que cuestan tiempo y dinero de los cuales platicamos en este artículo.
Para que esta estrategia funcione correctamente, no se puede dar la libertad de exagerar la medición y la dosificación correcta del ácido. Es sumamente crítico. Una alcalinidad más baja reduce la capacidad amortiguadora del agua, por lo que medir el ácido es indispensable para evitar problemas y también es importante que vierta el ácido correctamente con dilución previa. Es sorprendente que tan seguido se usa el ácido en exceso o de manera incorrecta, así como entre otros terribles hábitos comunes que cuestan tiempo y dinero de los cuales platicamos en este artículo.
Como ya sabemos, cada dosis de ácido reducirá la alcalinidad, ya sea levemente, si se usa esta estrategia correctamente, cada tercera o cuarta semana deberá volver a aumentar la alcalinidad con bicarbonato de sodio. Nuevamente, no necesitamos 80-120 ppm de alcalinidad en el verano si tenemos suficiente dureza de calcio para mantener el equilibrio del ISL. Esto podría ser contrario a lo que ha escuchado en la industria en el pasado, pero funciona de mejor manera.
Conclusión
La cantidad o concentración de dióxido de carbono en el agua determina el pH del agua. Cuanto más CO2 , menor será el pH y viceversa. El pH de una piscina aumentará naturalmente con el tiempo, gracias a que el CO2 sale del agua. Esto ocurre por sí solo y no significa que esté cometiendo errores en la manera que administra su piscina y química. La ley de Henry de la solubilidad de los gases explica por qué el CO2 busca estar en equilibrio con la atmósfera. Cuando se alcanza dicho equilibrio, el agua ha llegado a su valor máximo también conocido como "techo de pH". Este techo está determinado por la alcalinidad de carbonato en el agua.
Si desea ser proactivo con la química de la piscina, puede adoptar una estrategia de contención de pH, en lugar de perseguir e intentar controlar el pH, puede utilizar la dureza del calcio y la Ley de Henry a su favor y de esta manera predecir el aumento del pH de manera precisa y constante. Hacerlo puede ahorrarle mucho tiempo y dinero.
Nota: Una disculpa por la inconsistencia con la citación siguiente. Los autores y fechas de publicación de algunas de estas fuentes fueron difíciles de encontrar . Utilice los hipervínculos para encontrar las fuentes originales.
1 Artículo de investigación de la Universidad Estatal de Utah (2006). Dióxido de carbono y ácido carbónico.
2 Cabe señalar que el aumento de pH del cloro no estabilizado, como el hipoclorito de sodio (cloro líquido) o el hipoclorito de calcio (hipo cal) es temporal, porque cuando el HOCl se oxida o desinfecta, un subproducto del HCl compensa el pH alto. Fuente: Robert Lowry.
3 Textos de Química Libre. Ley de Henry.
4 La alcalinidad de carbonato es confusa, porque el término significa dos cosas. La alcalinidad de carbonato en sí misma es CO3, pero para propósitos del ISL y el techo de pH, "alcalinidad de carbonato" se refiere a la "alcalinidad corregida", que incluye bicarbonato, ya que simplemente podría eliminar un hidrógeno y aún tener un carbonato. La alcalinidad corregida es la alcalinidad total menos la alcalinidad del cianurato.
