Afecta la Temperatura el Rendimiento del Ácido Isocianúrico?

Hoy estamos discutiendo dos de los seis factores del ISL: temperatura del agua y ácido isocianúrico (CYA o AI). Específicamente, ¿será que temperatura más cálida afecta la capacidad del CYA para proteger la luz solar? Existe una creencia generalizada en la industria de que el clima más cálido significa que necesita un CYA más alto para proteger el cloro de la luz solar. Entonces le preguntamos a un experto líder sobre lo que realmente está sucediendo.
La luz del sol descompone el cloro libre

El ácido isocianúrico es una espada de doble filo, pero es necesaria para la mayoría de las piscinas al aire libre. Su principal beneficio y tal vez su único beneficio, es que protege el cloro de la degradación UV. Sin CYA en el agua, la luz solar directa puede destruir la mitad de su cloro libre en solo 45 minutos y otra mitad en los próximos 45 minutos. Eso significa que en solo 90 minutos, se redujo al 25% o menos del cloro con el que se comenzó. Sin embargo, el CYA se une al cloro y lo protege de la luz solar hasta que es hora de que el cloro se libere para matar u oxidar un contaminante.
El cloro que se une al CYA se llama isocianurato, y aparecerá en un kit de prueba de cloro libre. CYA es un arma de doble filo porque aunque están protegidos de la luz solar, los isocianuratos son mucho más lentos para desinfectar que el ácido hipocloroso libre (HOCl), por lo que CYA controla la fuerza (y la velocidad de eliminación) del cloro. De hecho, debido a que el CYA modera la fuerza del cloro, se ha hecho un argumento científico para usar una cantidad muy pequeña de CYA en una piscina cubierta para así reducir la tasa de consumo de cloro y los subproductos de desinfección.
El nombre del juego con estabilizador es tener suficiente protección solar, pero no demasiada en el punto que ralentice demasiado el desinfectante. Conocemos esta condición como sobre estabilización, y es un gran problema para las piscinas de todo el país.
Observe que dijimos que es la radiación ultravioleta de la luz solar la que descompone el cloro. La temperatura del agua no tiene nada que ver con eso. Pero existe una correlación entre la temperatura del agua y el consumo de cloro, y explicar esta correlación es la razón principal de este artículo en primer lugar.
Todas las reacciones químicas son más rápidas a temperaturas más altas.
No entendimos las razones químicas de por qué el cloro se agota más rápido en agua cálida que en fría. Entonces hicimos lo que solemos hacer: lo investigamos. En este caso, fuimos directamente con el mismo gurú de la química del agua, Richard A. Falk. Con el permiso de Richard, compartiremos algunos extractos de nuestro intercambio de correos electrónicos:
"Para las piscinas descubiertas, la pérdida de cloro es una combinación de descomposición de la luz solar, que es independiente de la temperatura, y la oxidación de sustancias orgánicas (generalmente de escombros). Y si el cloro activo (relación cloro libre/AI) no es lo suficientemente alto" En relación con los niveles de fosfato", entonces también puede haber demanda de cloro para matar las algas, apenas manteniéndose a raya ". - Richard A. Falk

Esto confirma algo de lo que sospechábamos. Las temperaturas más cálidas aceleran las reacciones químicas en general, y también aceleran la tasa de reproducción de algas, que es una amenaza constante para las piscinas de verano. Por otro lado está la demanda de oxidantes, que son principalmente compuestos orgánicos no vivos. Sabemos todo sobre los compuestos orgánicos no vivos, por eso abordarlos adecuadamente al complementar el cloro es nuestro segundo pilar de cuidado proactivo de piscinas . Cuanto más caliente es el agua, más rápido puede reaccionar el cloro (y todas las demás reacciones químicas), por lo que tiene sentido que el cloro se agote más rápido en aguas más cálidas. Puede mitigar la demanda de oxidantes abordando los compuestos orgánicos con enzimas.
Entonces, no, la protección solar del CYA o AI es independiente de la temperatura. No necesita más CYA cuando la temperatura aumenta, aunque los días de verano son más largos, con más horas de luz solar directa. Claro, esas horas adicionales de luz solar son importantes, pero la temperatura más alta no. Dicho esto, las piscinas a menudo experimentan una reducción más rápida del cloro por otras razones, como la demanda de oxidantes y la reproducción de algas, con las que un exceso de ácido no hace la diferencia. En todo caso, más CYA continuará desacelerando el cloro... así que cuando pruebe el cloro libre después de una semana, podría ser más, pero ¿fue realmente una victoria?
La descomposición del cloro en la luz solar depende del pH
Recientemente publicamos otro artículo sobre cómo el CYA supera el pH cuando se trata de controlar la fuerza y la velocidad del cloro (% HOCl). Según los datos disponibles, en ese artículo, postulamos que el pH es prácticamente irrelevante para la fuerza del cloro cuando el CYA está presente. Tampoco estamos solos en esta opinión, porque ni siquiera se nos ocurrió a nosotros. Simplemente compartimos el estudio del Dr. Stanley Pickens, la fuente original. Sin embargo, nunca discutimos que el pH fuera irrelevante para otros aspectos de la química del agua. Sabemos que el pH es el más impactante de los seis factores de ISL, por lo que es crítico para el equilibrio del agua. Y también sabemos que el pH determina el porcentaje de equilibrio de diferentes formas de alcalinidad.
Resulta que el pH realmente importa para la descomposición del cloro por la luz solar, porque a medida que aumenta el pH, también lo hace el porcentaje de ión hipoclorito (OCl-) que se disocia del CYA. En otras palabras, cuanto mayor sea el pH, más cloro se disocia del CYA (aunque sea la forma débil de cloro, OCl -, no el HOCl fuerte). Vea la línea verde en el gráfico (a la derecha) a continuación.
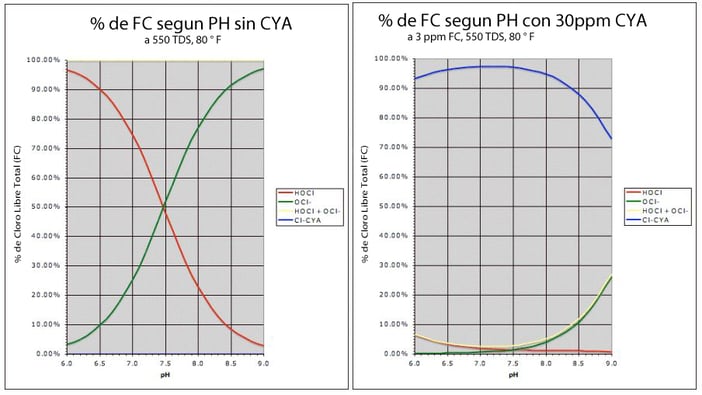
Como puede ver, el porcentaje de la línea roja (HOCl) se mantiene por debajo del 3% y disminuye gradualmente a medida que aumenta el pH. Pero la línea verde, el hipoclorito iónico (OCl-) sube a medida que aumenta el pH. Su aumento es directamente proporcional a la disminución de la línea azul, isocianurato. Esto significa que mientras el pH se eleva, más OCl - se desprende y queda expuesto a la luz solar. Esto es lo que dijo Richard:
"No olviden que la descomposición del cloro en la luz solar es MUY dependiente del pH porque el ión hipoclorito se descompone mucho más rápido que el ácido hipocloroso, y con el CYA en el agua, un pH más alto no genera mucho HOCl, pero consigue que el ión hipoclorito aumente mucho (ya que CL-CYA y OCl - están en equilibrio) ". - Richard A. Falk (colores añadidos por Orenda para que coincida con los gráficos anteriores)
Vaya, hay mucho que desempaquetar aquí, así que aquí hay algunos puntos clave:
- Esto todavía no cambia el hecho de que CYA domina el control de la fuerza del cloro (% HOCl) .
- Desde OCl - aparece en un kit de prueba de cloro libre, el nivel de cloro libre se caerá a un pH más alto debido a esta disociación de CYA.
- La razón por la cual las piscinas verdes que están eutrofizadas luchan por retener el cloro es porque tienen un pH muy alto. Algas consumen CO2, que atrae el CO2 de la solución y eleva el pH. Encontramos una piscina verde que midió 10.39 pH, que es más alto que el máximo en la tabla anterior. Ver video a continuación:
Luego Richard lanzó una bola curva que no esperábamos.
El cloro oxida lentamente el mismo CYA...
No se necesita parafrasear, esto es directamente de Richard:
"Además, en todas las piscinas que utilizan CYA, el cloro oxida lentamente el CYA . A temperaturas normales de la piscina, la pérdida de CYA es de alrededor de 3 ppm por mes y se requieren 2.5 ppm de cloro libre para oxidar 1 ppm de CYA, por lo que la oxidación de 3 ppm de CYA por mes se traduce a 7.5 ppm de cloro libre por mes o 0.25 ppm CL por día. Algunas piscinas muestran una mayor pérdida principalmente debido a una temperatura más alta y un pH más alto que acelera esta reacción. En los spas calientes que usan dicloro, la pérdida es típicamente de 5 ppm CYA por mes. sería 0,42 ppm CL/día. Algunas personas informan más, pero sospecho que eso incluye la pérdida de CYA por la dilución del agua ". - Richard A. Falk
Lo escuchó aquí primero, citado directamente de Richard, una fuente primaria que forma parte del comité ad-hoc de CMAHC para el ácido isocianúrico. Esto es algo que no sabiamos, y para ser sincero, no estamos seguros de que se haya procesado todavía. Teníamos la impresión de que el CYA se acababa de acumular y nada menos que bacterias especializadas y drenaje podrían reducirlo. Pero aparentemente el cloro mismo puede activar su protector, el ácido isocianúrico. Debido a que es una tasa de oxidación tan lenta, esto puede no ser realmente notable en la mayoría de las piscinas. Pero bueno, esto es realmente una buena noticia, porque poder reducir el CYA en las piscinas es algo bueno.
Conclusión
Escribimos este artículo para desacreditar la idea de que temperaturas más altas generan la necesidad de más AI para proteger el cloro. Mientras que el cloro se reduce más rápidamente en agua más caliente, eso no tiene nada que ver con la protección de la luz solar del AI. Más bien, esta mayor tasa de consumo de cloro se debe a una mayor demanda de oxidantes. La protección contra la luz solar es independiente de la temperatura. Entonces, no, no necesita niveles más altos de CYA en el verano. El sol es el sol, independientemente de la temperatura.
Tampoco debemos subestimar la velocidad de reacción del cloro. El agua más cálida significa que el cloro funciona más rápido, aunque esto es independiente de la protección solar.
Le damos el crédito a Richard Falk y le agradecemos por ayudarnos en este tema, ya que él es nuestra fuente principal y tuvo la amabilidad de tomarse el tiempo para responder nuestras preguntas. En el camino, aprendimos cosas fascinantes sobre el CYA que nunca supimos, como que el pH siendo más alto significa que el cloro se puede consumir más rápido. Niveles de pH más altos producen más disociación de OCl – por causa de CYA, y esa disociación de OCl - cause vulnerabilidad a la degradación luz solar. Esto no debe confundirse con que el cloro que es más débil (% HOCl ), porque el cloro no es realmente más débil a mayores niveles de pH con CYA en el agua.
Si tiene preguntas, ¡nos encantaría saber de usted! Comente abajo.
