Conteniendo el pH en Lugar de Controlarlo

La escasez en el mercado de suministro gracias a COVID-19 ha afectado de manera grave al negocio de las piscinas. De manera paralela a la falta de cloro, ahora se acerca la escasez de ácido para nuestra industria. En este artículo le explicaremos cómo reducir la demanda de ácido de su piscina mediante un mejor equilibrio en la química de su piscina y aprenderá que es más conveniente contener el nivel del pH en un cierto nivel límite en lugar de solo perseguirlo tratando de ajustar su valor específicamente. El resultado? Un menor mal uso de químicos y una quimica mas predecible.
Cubierto en este artículo:
- ¿Cual es la demanda de ácido?
- Conteniendo el pH en lugar de controlarlo
- Cómo reducir la demanda de ácido
- Conclusión
Cuál es la demanda de ácido?
A la cantidad de ácido que su piscina necesita para mantener el equilibrio químico del agua se le conoce como demanda de ácido. La demanda de ácido es similar a la demanda de cloro, ya que su piscina básicamente consume el químico. En Orenda, hemos observado una tendencia al uso excesivo de ácido por parte de la mayoría de las personas en la industria. De hecho, el abuso del ácido es nuestro primer mal hábito identificado en nuestro artículo "6 malos hábitos a cambiar". Existen varias razones por las cuales el ácido es sobre usado.
Porque se abusa del ácido
Primero que nada, si se siguen las guías y pautas del tratamiento de piscinas a la manera tradicional, se pueden provocar problemas. Claro que generalmente los rangos de química recomendados pueden funcionar en el verano... pero qué sucede durante la primavera, el otoño y el invierno?. El hecho es que tratar de mantener ciertos parámetros químicos dentro de los rangos sugeridos por libros de texto puede ser imposible durante gran parte del año. 1 Particularmente, si se trata de mantener un pH entre 7.2 y 7.8, e idealmente entre 7.4 y 7.6 será necesario violar otros parámetros químicos (por ejemplo, una alcalinidad más baja) o tratar el agua de la piscina constantemente con ácido para combatir el aumento natural del pH. A esto es lo que nos referimos cuando decimos tratar de controlar o perseguir el pH. Entonces, por que los libros nos recomiendas mantenernos en estos niveles de pH? Los libros argumentan las siguientes dos razones: comodidad del bañista y la fuerza del cloro. Hablemos un poco más de esta última razón.
Se supone que el pH controla la fuerza del cloro, como nos han enseñado a todos. Y de hecho lo hace, para una piscina cubierta o cualquier piscina que no tenga ácido isocianúrico (CYA) o estabilizador en el agua. Sin embargo las cosas cambian cuando existe este químico en el agua. La relación de proporción de cloro libre con ácido isocianúrico determinara la fuerza del cloro. El porcentaje de cloro fuerte (ácido hipocloroso o HOCl) es prácticamente el mismo cuando se tiene un pH de 7.0 que cuando se tiene uno de 8.5 cuando solo hay 30 ppm de CYA en el agua. Se observa en la siguiente gráfica:

La gráfica de la izquierda es lo que nos enseñan y educan en los libros de texto. Pero la mayoría de las piscinas al aire libre en Estados Unidos tienen al menos algo de CYA. Podemos comparar la línea roja en ambos gráficos, la cual representa el porcentaje de ácido hipocloroso en el agua (cloro fuerte). ¿Alguna diferencia? Esto ocurre porque cuando CYA está en el agua, la gran mayoría del cloro se une con este compuesto. Y el pH no dicta la fuerza del cloro cuando está unido con el CYA (los isocianuratos, representados por la línea azul). Por tanto, el argumento de que el pH controla la concentración del cloro, a nivel práctico, solo se aplica a las piscinas no estabilizadas.
La tercera razón por la que el ácido se usa en exceso en las piscinas es porque el ácido se considera la primera (y más fácil) opción para remediar las decoloraciones y los defectos del yeso. Bien o mal, la costumbre ha sido usar ácido para solucionar los problemas del yeso. Tiene sarro? Agregue ácido. Algo de decoloración? Ácido. Polvo de yeso? Ácido. Marcas en las superficie, rayas y otros problemas importantes? Agregue MUCHO ácido. Y aunque el ácido puede ayudar con algunos problemas, siempre debería de ser la última opción debido a su agresividad. Resolver el problema del ISL debe ser su primera prioridad. Esto puede implicar un poco de ácido diluido para ajustar los parámetros químicos, pero no vierta ácido en la piscina para quemar las imperfecciones. Hay una gran diferencia!
Conteniendo el pH en lugar de controlarlo
En lugar de intentar controlar el pH, intente contenerlo. Por su propia naturaleza, el valor del pH cambia fácilmente cuando se agrega cualquier cosa al agua y, naturalmente, también aumenta con el tiempo. Tratar de controlarlo es inútil, especialmente cuando se trata de controlarlo dentro de parámetros estrictos como 7.4 a 7.6. Para mantener un pH dentro de ese rango, se deben de vencer las leyes de la física. Sin un controlador químico automático y un alimentador de ácido, le deseamos buena suerte.
Porque el pH sube naturalmente?
Tenemos otros artículos acerca de las causas de un pH alto y aún más específicamente de por qué el pH aumenta de forma natural. En resumen, el pH aumenta naturalmente en las piscinas porque el agua de la piscina está sobre carbonatada en comparación con el aire que respiramos. Este fenómeno se explica por la Ley de la física de Henry. 2 En resumen, la Ley de Henry establece que a cierta temperatura, la solubilidad de un gas en un líquido es directamente proporcional a la presión parcial de ese gas sobre el líquido. En otras palabras, la presión del gas estará en equilibrio proporcional dentro y fuera del agua. En lo que respecta al pH, el gas que está en juego es el dióxido de carbono (CO2). ¿Por qué? Porque mientras que el pH nos dice la concentración de iones de hidrógeno (H+), la cantidad de CO2 disuelto en el agua afectará dicha concentración y por lo tanto el pH del agua. Cuanto más CO2 se disuelva, menor será el pH. Cuanto menos CO2, mayor es el pH. Aquí hay un gráfico traducido de Robert Lowry para ayudar a visualizar el proceso:
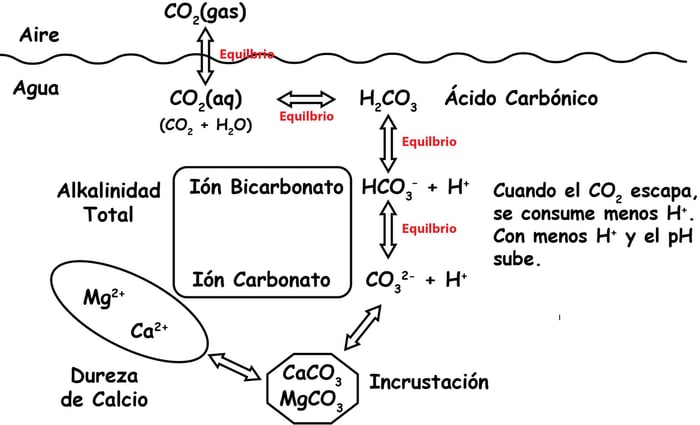
Gráfico de Robert W. Lowry. Con aprobacion.
Otra analogia, una botella de cerveza.

En la botella, la cerveza no tiene burbujas. Esto se debe a que el CO2 está en equilibrio dentro de la botella. Pero cuando se abre la botella, la presión se libera y de repente aparecen burbujas dentro de la bebida que suben a la superficie. Lo que está presenciando es la Ley de Henry en acción. El CO2 se escapa de la cerveza rápidamente para igualarse con el CO2 en el ambiente. Eventualmente, se alcanza el equilibrio y la cerveza deja de ser carbonatada (lo que arruina el sabor)
Las mismas leyes de física se aplican en la piscina. Simplemente no podemos ver las burbujas y la superficie de la piscina es mucho mayor.
Entonces, el pH aumenta naturalmente porque el CO2 debe escaparse del agua en busca de equilibrio con el ambiente. Sabiendo esto, ¿cómo se supone que debemos controlar el pH exactamente? Solo para recordarle, esta es una ley de la física... no una sugerencia. La única forma de controlar realmente el pH, como se mencionó anteriormente, es con la automatización química, ya sea un alimentador de ácido o un inyector de CO2, o ambos. En cualquier caso, está tratando de forzar el pH a estar en algún lugar donde naturalmente el pH no quiere estar. Cuando se alcanza el equilibrio de CO2, el pH naturalmente no puede aumentar más. A esto lo llamamos el techo de pH y, dadas ciertas temperaturas, la alcalinidad de carbonato de su agua determina este techo:
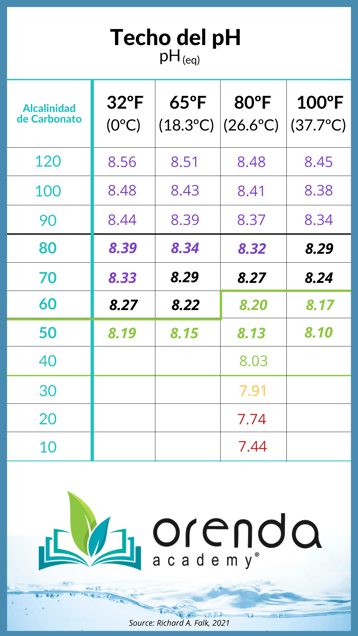
Fuente: Richard A. Falk. Los valores de la tabla son para varias temperaturas del agua (ºF).
Cómo contener el pH
Dado que controlar el pH es un objetivo inútil, la mejor alternativa es contenerlo. La contención es bastante simple con la ayuda de la calculadora Orenda del ISL Ajuste su alcalinidad para establecer un techo de pH que pueda manejar. 3 Luego, ajuste la dureza del calcio lo suficientemente a un nivel alto para que en su nuevo objetivo de alcalinidad, su ISL permanezca equilibrado entre el pH deseado más bajo posible y el techo de pH (según la tabla anterior). Suena más complicado de lo que realmente es. Podemos utilizar el siguiente ejemplo:
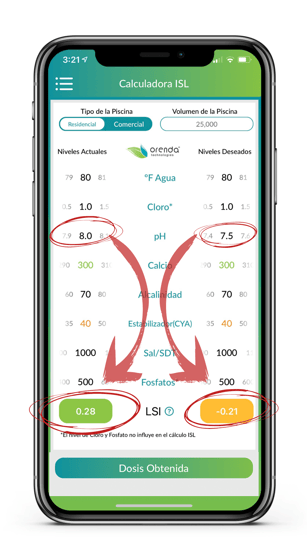
Observemos como la alcalinidad es menor que los niveles recomendados entre 80-120 ppm. Esto es intencional, de modo que cuando el pH sube al nivel máximo (el techo), el ISL permanece verde. Un nivel mayor de alcalinidad, con un pH de 8,0, provocaría sarro de carbonato. La única corrección que se necesita en este ejemplo es reducir el pH lo más bajo posible a un nivel del ISL amarillo sin que este se vuelva rojo. Este umbral es lo que en Orenda le conocemos como eI piso del pH. Entonces tendremos un piso y un techo del pH. Estos son los valores bajos y altos de su pH mientras es contenido. Los parámetros pueden cambiar a medida que cambia la temperatura del agua (principalmente con la dureza del calcio), pero el concepto es el mismo independientemente de la temperatura. La analogía que usamos es un elevador que contiene su pH.
El ritmo de liberación de CO2 y el aumento del pH son una función cuadrada
Hay otra cosa importante que debe saber sobre la emisión del CO2. Cuanto más se acerca el agua al equilibrio del CO 2 (techo de pH), los gases de emisión del CO2 son exponencialmente más lentos. Es una función
al cuadrado. Entonces, puede tomar unos minutos para que el pH aumenta naturalmente de 7.2 a 7.3, pero podrían tomar días para que suba de 7.9 a 8.0. En otras palabras, esto significa que es posible que el agua nunca alcance su límite de pH en una semana. Si tiene un sistema de sal, podría hacerlo, pero es posible que las piscinas de cloro líquido y las piscinas hipocalóricas no lo logren. Aunque existen más factores, solo tiene que saber que
la velocidad del aumento natural del pH disminuye en función a una raíz cuadrada.
La captura de pantalla de la calculadora anterior tenía este aspecto en cuenta, mostrando el pH de solo 8.0, en lugar de su techo más preciso entre 8.13 y 8.20. Utilice esta consideración del aumento del pH a su favor. Le da tiempo y hace que la subida del pH sea más predecible.
En esencia, la contención del pH se logra construyendo su estrategia del ISL en torno a un pH que aumenta consecutivamente. Siempre que no corrija el pH a un valor demasiado bajo, su pH debería aumentar al mismo ritmo semana tras semana, asumiendo la misma alcalinidad.
Entonces, contener el pH tiene que ver con el marco del ISL alrededor del pH. ¿A quién le importa cuál es el pH entre el suelo y el techo? Si sabemos el límite a lograr! Y la fuerza de su cloro en una piscina con CYA ya no está relacionada con el pH. Así que déjelo subir, porque el pH aumentará de todos modos.
Cómo reducir la demanda de ácido
En comparación con la práctica tradicional de tratar de controlar (o perseguir) el pH, contener el pH a nuestra manera puede ahorrarle una enorme cantidad de ácido y bicarbonato de sodio. Piénselo. Sus dosis de ácido serán predecibles y, debido a que tiene menos alcalinidad en el agua, las dosis también serán más pequeñas. Además, el uso de menos ácido significa que se neutraliza menos alcalinidad, por lo que tampoco necesitará tanto bicarbonato. Estará haciendo microajustes, no ajustes criticos.
Además de la estrategia de contención en sí, aquí hay algunas otras formas de ahorrar ácido:
- Siempre diluya el ácido. No diluir significa que el ácido puede llegar al fondo de la piscina y dañar las superficies de cemento/yeso, lo que neutralizará el ácido y provocará un pH aún más alto en poco tiempo.
- Mida siempre el ácido. No, su piscina de 20,000 galones probablemente NO necesita medio galón para hacer una corrección de pH. Conozca la alcalinidad y el volumen de su piscina, y la aplicación Orenda le dirá exactamente cuánto ácido se necesita. A menudo es menos de lo que cree que necesita.
- Si comete un error en la dosis de ácido, procure que sea menos que más. Nunca cause una sobredosis de ácido.
- Conozca la química del agua del llenado. Si tiene alta alcalinidad o pH alto empezando desde el agua de llenado, el ácido será util. Si tiene poca alcalinidad y pH bajo en el agua de llenado, quizás un sistema de CO2 podría ser mejor para su piscina. Sólo tenga en cuenta el problema de las algas y los alimentadores de CO2 en las piscinas al aire libre (las algas se alimentan de CO2).
- Si tiene automatización química, considere una alimentación programada de ácido, en lugar de "detectar y dispensar". Esto significa que su piscina siempre obtendrá la cantidad exacta de ácido necesaria para volver al pH deseado, en lugar de alimentarlo con ácido hasta que la sonda de pH reconozca un cambio. Ah, y también, alimente ácido a la velocidad de alimentación más lenta posible para maximizar la dilución. Si usted es un operador comercial que lucha por mantener el pH y la alcalinidad, vale la pena conversar más con nosotros. Solicite una clase de asesoría gratuita aquí.
- Cambie el hábito de usar 16 oz. de ácido muriático por cada galón de cloro líquido. No necesita tanto ácido, porque técnicamente el cloro líquido solo eleva temporalmente el pH. Una vez que mata u oxida, el pH vuelve a bajar porque el cloro libera una cantidad casi igual de ácido muriático (HCl) para neutralizarse. Dicho esto, un poco de ácido será más que necesario un poco antes o después de agregar cloro líquido. En lugar de 16 oz. de ácido, pruebe con 8 oz, o incluso 4 oz.
- Deje de usar ácido como primer recurso cuando se trata de problemas con el yeso. Pruebe los parámetros y ajuste el ISL. Sí, el ajuste del ISL puede involucrar ácido diluido para hacer un ajuste de pH o alcalinidad, pero eso no es lo mismo que tirar ácido en una piscina para limpiar una superficie. Un uso tan intenso de ácido puede tener su lugar, pero no es la primera opción.
Conclusión
Tenemos la tendencia a usar ácido en exceso en nuestro negocio. Ahora que el cloro y el ácido están sufriendo de escasez, se nos presenta la oportunidad de pensar un poco diferentes y usar diferentes estrategias. La manera tradicional de tratar la piscina químicamente es seguir ciertos niveles como mantener el pH entre 7.2 y 7.8. Pero si tiene CYA en su piscina, estamos seguros que esta ya no es necesario.El pH sigue siendo importante, por supuesto, pero deberíamos contener el pH en lugar de intentar controlarlo.Una vez que aceptamos el hecho de que el pH aumentará naturalmente debido al CO2 y su equilibrio (Ley de Henry), podemos optar por no estar atados a parámetros de pH tan estrictos. Generalmente, se desea permanecer entre 7.5 y 8.0, aunque la mayoría de las piscinas tendrán un techo de pH de alrededor de 8.1 o 8.2. Este artículo puede usarse como guía para como bajar el techo del pH simplemente reduciendo la alcalinidad de carbonato para luego ajustar los otros parámetros del ISL, mientras se mantiene todo en equilibrio.
Este artículo no habla de mitos e ideas hipotéticas. Funciona y lo hemos probado una y otra vez. Obedezca la física y el agua se comportará de manera predecible. Más allá de simplificar su rutina de mantenimiento, ahorrará mucho en ácido y bicarbonato de sodio, porque ya no estará persiguiendo el pH. Deje de gastar dinero y productos químicos tratando de obligar al agua a mantener un pH que no puede mantener. En su lugar, adopte la física, contenga el pH y déjelo subir cada semana antes de restablecerlo.
La cantidad de ácido que se ahorrará puede ser sorprendente.
1 Es por eso que enseñamos primero el ISL, luego la química de rango.
2 Textos de Química libre. Ley de Henry. Actualizado en febrero de 2021.
3 Ajuste su alcalinidad total (AT) en la aplicación, pero el techo de pH se basa en la alcalinidad de carbonato. Al implementar esta estrategia de contención, tome un tercio de su ácido isocianúrico y reste eso de su AT (0.33 x CYA).

